-
처음 위치
-
이중가닥 절단과 수선이중가닥 절단과 수선 하위섹션 토글하기
-
조작된 핵산분해효소조작된 핵산분해효소 하위섹션 토글하기
-
적용
-
전망과 한계
-
참고 문헌
유전체 편집(영어: genome editing, gene editing) 또는 조작된 핵산분해효소를 이용한 유전체 편집(genome editing with engineered nuclease, genome engineering)은 인공적으로 조작된 핵산분해효소 혹은 유전자 가위를 이용해 유전체로부터 DNA가 삽입, 대체 혹은 결실되는 유전 공학의 일종이다.
핵산분해효소는 유전체 상의 원하는 위치에 특정한 이중가닥절단(Double-stranded break, DSB)을 일으키게 되고, 그 절단은 세포의 자체적인 기작에 의해 상동재조합(Homologous Recombination, HR) 또는 비상동말단연결(Non-homologous end joining, NHEJ)의 방식으로 수선된다. 최근 주로 이용되고 있는 조작된 핵산분해효소는 크게 4가지가 있다 : ZFNs (Zinc Finger Nucleases), TALENs (Transcription Activator-Like Effector Nucleases), the CRISPR/Cas system, 그리고 메가핵산분해효소 (meganucleases).[1][2][3]
- 일부 생물체에서만 작용하는 한계가 있다.
- 엄격한 선별 과정을 필요로 하므로, DNA상에 선별을 위한 특이적인 서열을 추가적으로 넣어주어야 한다.
- 다소 불충분한 부분이 있다.
그러므로, 조작된 핵산분해효소를 이용한 유전체 편집은 앞서 설명한 것들의 단점을 극복하고 상대적으로 간단하게 이용 가능한 접근법이라고 할 수 있다.
이중가닥 절단과 수선[편집]
유전체 편집에서 뉴클레아제(핵산분해효소) 작용의 핵심은 DNA 이중 가닥 절단·수선 메커니즘에 대한 이해가 필요하다. 이중가닥 절단은 DNA 두 가닥 사이의 약한 수소 결합을 분해하는 특정 효소가 작용하여 일어난다. 일반적으로 이중가닥 절단의 수선에 대해 2가지 경로가 알려져 있다. 상동재조합(Homologous Recombination, HR) 또는 비상동말단연결(Non-homologous end joining, NHEJ)이 그것이다. 상동재조합과 비상동말단연결은 모두 DNA 수선 기작이지만, 그것이 일어나는 시기는 다르다. 비상동말단연결은 주로 G1 시기에 일어나며, 상동재조합은 DNA가 복제되는 S기나 G2기에 일어난다. 대부분의 분화된 세포들은(뉴런등) 복제를 하지 않기 때문에 상동재조합이 일어나기 어렵다.[5]
비상동말단연결 (NHEJ, Non homologous end joining)[편집]
비상동말단연결은 마이코박테리아 (mycobacteria)의 이중가닥 절단부에서 50%의 확률로 돌연변이를 유발한다고 할 만큼 오류를 유발하는 수선방식이다.[6] 또한 비상동말단연결의 낮은 정확도는 백혈병에서 변이의 축적과 관련이 있다.[7] 그러므로, 만일 다양한 샘플에서 원하는 유전자에 이중가닥절단을 만들 수 있다면, NHEJ의 부정확성을 통해 그 위치에 쉽게 변이가 만들어질 수 있다.비상동말단연결은 이중가닥 절단의 끝을 직접적으로 연결해주기 위해 다양한 효소를 이용한다. 이중가닥절단이 일어나면 DNA의 이중가닥 절단 말단 부분에 붙는 Ku70/80 이형이형다량체가 DNA 가닥에 붙게 되고, 이 복합체는 DNA-PKcs를 불러들인다. DNA-PKcs는 자기인산화를 통해 Artemis가 DNA 끝을 가공하는데 유리하게 해준다. 마지막으로 XRCC4/DNA ligase IV 복합체를 이용하여 DNA 양 끝을 라이게이션을 통해 수선이 일어난다.[5]
상동재조합 (HR, Homologous recombination)[편집]
반면, 상동재조합의 경우 상동성 있는 서열을 포함한 DNA 공여체가 수선의 주형으로 이용되므로, 관심 있는 유전적 부분에 원하는 변이를 만들어낼 수 있다는 장점을 가진다. 상동재조합의 경우 DNA 이중가닥 절단이 일어나면, PARP1 이 DNA 이중가닥 절단 부위에 붙게되며, MRN 복합체(MRE11, Rad50, Nbs1)를 불러들인다. MRN 복합체는 DNA 이중가닥 말단에 붙게 되고, 이후 인산화 된 CtIP를 불러들인다. 인산화 된 CtIP는 MRE11의 앤도뉴클레아제 부분을 활성화 시킨다. 뿐만아니라 CtIP는 BRCA1, BARD1과 함께 상동재조합 과정의 초기단계를 중재한다. 활성화 된 MRE11는 3' 말단의 짧은 단일가닥 DNA 꼬리를 만들며, EXO1과 DNA2 / BLM은 DNA 절단된 가닥의 광범위한 절단을 통해 긴 ssDNA 가닥을 만들게 되며, 생성된 ssDNA에 RAD51이 붙게 된다. RAD51 필라멘트는 DNA 가닥 사이의 침입을 통해 상동재조합을 유도한다.[5]
메커니즘적으로는 매우 다름에도 불구하고, 상동재조합을 기반으로 하는 유전체 편집은 유전자적중법 (Gene targeting)과 매우 유사한 방식으로 진행된다. 그러나, 재조합의 빈도는 이중가닥절단이 만들어지고 상동재조합 기반의 수선이 일어날 때 1000배가량 높아진다. 왜냐하면, 보다 효율적이고 positive, negative 선별과정을 필요로하지 않기 때문이다.[8]
이러한 것들을 바탕으로 할 때, 유전체 내 특정 위치에 이중가닥절단을 만들면, 세포의 자체적 수선기작을 활용해 원하는 변이를 얻어낼 수 있다.
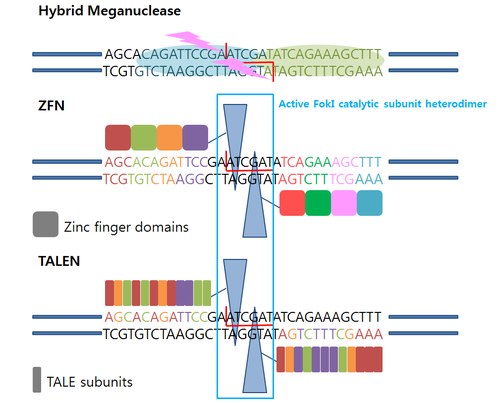
조작된 핵산분해효소[편집]
메가핵산분해효소 (meganuclease)[편집]
1980년 대 후반 발견된 메가핵산분해효소는 긴 DNA 서열(14~40 염기쌍)을 인식하고 절단하는 앤도뉴클레아제 효소이다. 가장 잘 알려진 메가핵산분해효소는 LAGLIDADG계열의 단백질로 아미노산 서열을 이용하여 명명하였다. 메가핵산분해효소는 미생물종에서 흔히 발견되는데, 인식서열이 매우 길기 때문에(>14bp) 특이성이 매우 높다.[9][10] 이것이 유전체 편집에 메가핵산분해효소를 이용하게 한 결정적인 요인이다. 그러나, 유전체 내 모든 서열을 대상으로 하기에는 부족하다. 이를 극복하기 위해 돌연변이유발 및 고해상도 스크리닝 기법을 통해 특정 서열을 인식하도록 한 메가핵산분해효소의 변종을 만들기 위한 시도가 있었다.[10] 뿐만 아니라, 다양한 메가핵산분해효소들을 섞어 새로운 서열을 인식할 수 있는 잡종 효소를 만들기도 하였다.[11]
인식하는 서열의 특이성이 높다는 점은 메가핵산분해효소가 다른 방식에 비해 세포에 독성을 낮게 유발한다는 장점을 갖게 한다.[10] 그러나, 가능성이 있는 모든 서열에 대해 특이적으로 메가핵산분해효소를 제작하는 것은 비용과 시간 소모 측면에서 효율적이지 못한, 장점과 단점이 공존하는 기술이다.
징크핑거 핵산분해 효소 (ZFN, Zinc finger nuclease)[편집]
메가뉴클레아제와 다르게 징크핑거 핵산분해 효소와 탈렌 기술은 염기서열 비특이적인 DNA를 절단하는 도메인을 기반으로하며, 이 DNA 절단 도메인은 징크핑거와 탈렌(TALEs, transcription activator-like effectors)과 같은 DNA를 인식하는 펩타이드와 연결될 수 있다. 즉, DNA 결합 도메인과, DNA 절단 도메인을 따로 가지고 있다. 이러한 방법을 알아 내기 위한 첫 번째 단계로 DNA 인식 부분과 절단 부위가 서로 분리된 핵산 분해 효소를 발견하는 것이다(type II S endonuclease).[12] 이러한 효소의 절단 부분은 DNA를 인식할 수 없기 때문에 특이적이지 않다. 따라서 이 부분을 높은 특이성으로 DNA를 인식하는 펩타이드와 연결하여 서열 특이적인 핵산분해효소를 이용할 수 있다. 그 중 징크핑거 핵산분해 효소는 비특이적인 DNA 절단 도메인과, 징크핑거 모티프의 DNA 결합 도메인을 결합하여 이용하는 기술이다.
징크핑거 모티프는 여러 전사 인자에서 발생한다. 모든 인간의 단백질의 8%에서 발견되는 아연 이온은 3차원 구조의 구성에 중요한 역할을 한다. 전사 인자에서 단백질-DNA의 상호 작용 부위에 위치하고 있고 각 핑거의 c-말단 부분은 DNA 서열을 특이적으로 인식한다.
인식하는 염기 서열은 약 3 염기쌍으로 짧지만 서로 다른 인식 부위를 가진 6~8개의 징크 핑거를 조합함으로써 약 20 염기쌍에 특이적인 단백질을 얻을 수 있다. 따라서 특정 유전자의 발현을 조절하는 것이 가능해 진다. 이렇게 만든 단백질을 핵산 분해 효소의 도메인과 융합시켜 원하는 염기서열의 DNA의 절단을 유도하고, 이런 단백질들을 게놈 연구의 도구로 사용하는 것이 가능하다.[13]
보통의 징크핑거 핵산분해 효소는 두 개의 DNA 결합 단백질( 3 ~ 6 개의 zinc finger를 포함 ) 과 핵산 분해 효소인 Fok1의 제한 도메인을 결합시킨다. 두 단백질은 몇 개의 뉴클레오타이드가 떨어져 있는 두 개의 DNA 서열을 인식한다. 두개의 징크핑거 단백질을 각각의 서열에 연결하면 두 개의 Fok1 도메인이 가까워진다. Fok1은 핵산 분해 효소 활성을 갖기 위해 이량체가 필요하며 각 핵산 분해 효소 파트너가 독특한 DNA 염기 서열을 인식함에 따라 특이도가 증가한다. 이러한 효과를 높이기 위해서 Fok1은 이질이량체만 기능 할 수 있도록 조작되었다.[14][15]
특정 서열에 대한 징크핑거 뉴클레아제를 설계하기 위해 여러 접근법이 사용된다. 가장 널리 알려진 것은 징크핑거 유닛을 알려진 특이성과 결합하는 것이다. 최적의 특이성과 세포 내성을 가진 조합을 확인하기 위해 박테리아나 효모 또는 동물 세포를 이용한 기술이 개발되었다. 징크핑거 뉴클레아제 활성의 직접적인 DNA 전체 특성은 보고되지 않았지만 세포에서 이중 가닥 DNA 절단의 총 수를 측정하는 분석은 징크핑거 뉴클레아제를 처리한 세포에서 24bp를 인식하여 1에서 2개의 절단이 일어나는 것을 확인하였다.
이질이량체의 작용은 동종이량체의 원하지 않는 활성을 피함으로써 DNA 이중가닥 절단의 특이성을 증가시킨다. 징크핑거 핵산분해 효소와 탈렌구조의 핵산 분해 효소는 비슷한 성질을 가지고 있지만 가장 큰 차이는 DNA를 인식하는 펩타이드에 있다. 징크핑거 핵산분해 효소는 Cys2-His2, 탈렌은 탈이펙터(Transcription activator-like effector)의 구조에 의존한다.[16] 이들 펩타이드 도메인을 인식하는 DNA는 둘 다 단백질에서 자연적으로 발견되며, Cys2-His2 징크핑거는 3bp 떨어져 있는 반복서열에서 일어나고 전사 인자와 같은 다양한 핵산 상호 작용 단백질에서 다양한 조합으로 발견된다. 징크핑거 도메인의 각 핑거는 완전히 독립적이며 하나의 핑거가 결합하는 서열은 이웃 핑거의 영향을 받는다. 한편, 탈이펙터는 아미노산과 인식된 뉴클레오타이드 사이의 1 : 1 비율로 인식한다. 징크핑거와 탈이펙터는 모두 반복적인 패턴으로 발생하기 때문에 다양한 조합을 시도하여 다양한 서열 특이성을 만들 수 있다. 징크핑거는 모듈 조립, OPEN( 낮은 활성의 도메인, 3중 뉴클레오타이드를 강하게 인식하는 펩타이드 조합, 박테리아 시스템에서 마지막 타겟), 징크핑거 라이브러리, 박테리아 하이브리드 스크리닝 등이 특이적인 뉴클레아제를 만드는데 사용되었다.
탈렌 (TALEN, Transcription activator-like effector nuclease)[편집]
탈렌(TALEN, Transcription activator-like effector nuclease)는 전사활성화 인자 유사 이펙터의 DNA 결합 단백질 도메인과 제한효소를 붙여 가공한 인공 제한효소이다. DNA 결합 부분인 탈이펙터는 Xanthomanos 박테리아의 avirulence gene인 avrBs3로부터 처음 발견되었다[17]. TAL 이펙터는 33개에서 34개의 반복된 아미노산 서열이 반복된 형태로 이루어져 있으며, 도메인(RVD, Repeated variant domain)이 약 9개 정도 반복된다. 도메인 하나당 한 개의 뉴클레오타이드를 인지 할 수 있으며, 12-13번째 아미노산 서열 에 따라 특이적인 DNA 서열과 결합 할 수 있다(HD->Cytosine, NI->Adenine, NG -> Thymine, NN -> Guanine).[18] 탈이펙터(TALE)는 표적부위 내의 단일 DNA 가닥을 인식한다. 따라서 탈렌은 두개의 탈이펙터를 이용하며, 이형이량체의 형태로 작동한다. 표적 부위 사이의 거리는 12-14 뉴클레오타이드 정도가 적당하다. 탈 이펙터 도메인을 이용하여 유전체 편집기술의 이용할 수 있다. 예를 들면, 탈이펙터의 DNA 결합 부분과, 제한효소인 Fok I의 촉매작용부위를 결합하여 만든 탈렌을 이용하면, DNA 이중가닥 절단이 일어난다. 주로 비상동말단연결을 통해 DNA 수선이 일어나므로, 타겟 위치의 비특이적인 삽입, 결실등이 일어난다. 그러나 탈렌은 징크핑거와 비교하여 DNA 결합 특이성이 더 높고, 오프-타겟 효과가 낮으며, DNA 결합 도메인이 더 간단하다. 하지만 탈 이펙터의 크기가 크고, 반복된 서열이 존재하기 때문에 탈렌의 오픈 리딩프레임을 렌티바이러스 시스템을 통해 형질도입하게 되면 템플릿의 전환이 일어나는 한계가 있다.[19] 이 한계를 극복하기 위해 BuDs와 같은 alternative TALE-like 스캐폴드를 사용한다.[20]
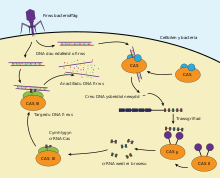
크리스퍼 유전자 가위 (CRISPR, Clustered regularly interspaced short palindromic repeats)[편집]
CRISPR (Clustered Interspaced Short Palindromic Repeats)은 박테리아가 바이러스로부터 보호 할 수 있는 일종의 획득 된 면역력으로 사용하는 유전 요소이다. 박테리아에 파지나 플라스미드가 들어오게 되면 외부 DNA 조각(protospace)을 박테리아 유전체 속 반복 서열 사이에 넣게된다. 이 반복된 서열을 CRISPR이라고 한다. CRISPR array에는 두개의 RNA가 암호화되어 있는데, 하나는 crRNA(CRISPR RNA)이고, 다른 하나는 tracrRNA(trans activating CRPSPR RNA)이다. crRNA는 protospace 부분에서 전사되며, tracrRNA와 결합하여 3차 구조를 형성한다. 두 종류의 RNA는 핵산분해효소가 외부 DNA를 인지하고 자를 수 있도록 도와준다.[21] CRISPR 시스템에서 crRNA와 tracrRNA를 합쳐서 하나의 RNA만을 사용하도록 gRNA를 새롭게 프로세싱 하였다. gRNA는 20bp 정도의 서열 인식범위를 가지고 있다. gRNA를 사용하면 하나의 RNA를 이용하므로 좀 더 간단하게 유전체 편집을 할 수 있다. 그러나 한가닥의 gRNA를 사용하는 것보다 crRNA와 tracrRNA 두가지를 사용한 CRISPR 기술이 더 효율이 좋다고 알려져 있다. CRISPR 시스템을 통해 외부 DNA를 자르기 위해서는 가이드 RNA와 핵산분해효소의 존재 뿐만 아니라 PAM 서열이 필요하다. PAM 서열은 protospacer associated motif로써 CRISPR 시스템에서 핵산가수분해효소가 타겟 DNA를 인지하도록 도와주는 서열이다.[22] 가장 많이 사용되고 있는 CRISPR-Cas9 시스템의 PAM서열은 'NGG'이고, PAM 서열을 가지는 외부 DNA의 gRNA를 통해 20bp 정도 타겟팅하면 cas9이 17~18bp 사이를 자르게 된다[23]. gRNA에 의해 특정 유전자를 표적하게 되면 핵산가수분해효소에 의해 이러한 서열을 처리하고 일치하는 DNA 서열을 절단한다. 절단된 DNA는 수선 기작에 의해 돌연변이를 유발하게 된다.
| 위키뉴스에 이 문서와 관련된 기사가 있습니다. |
| 징크핑거 핵산분해 효소 |
|
|
|
| 탈렌 |
|
|
|
| 크리스퍼 유전자 가위 |
|
|
|
적용[편집]
지난 몇 십 년 동안, 효율적인 유전체 편집은 때로는 임상적 흥미를 넘어서 식물에서 동물에 이르기까지 다양한 범위에서 발전해왔다. 그리고 유전체 편집은 연구실에서의 표준 실험 전략으로 자리 잡고 있다.[24] 최근 만들어진 ZFN-매개의 쥐 (Rat), 제브라 다니오 (Zebrafish), 옥수수 그리고 담배 (Tobacco) 유래 변이체들은 그 중요성이 입증되고 있고, 관련한 연구가 빠르게 이루어지고 있다.
조작된 핵산분해효소를 이용한 유전체 편집은 식물이나 동물의 유전자 기능 연구에서 인간의 유전자 치료에 이르기까지 생명과학의 많은 분야에 기여할 것으로 기대된다. 예를 들어, 고유 기능을 하도록 세포나 유기체를 조작하는 것을 목적으로 하는 합성 생물학 (synthetic biology) 분야에서 조작된 핵산분해효소는 유전인자의 첨가나 제거에 이용될 수 있다. 이는 나아가 복잡한 시스템을 만드는 데 기여할 수 있다.[24] 더불어, 조작된 핵산분해효소를 이용하여 줄기세포를 이용한 유전자 기능 연구도 가능하다.
유전체 편집을 적용할 수 있는 일들을 나열해보면 다음과 같다.
- 특정 서열의 유전자 변이
- 염색체 재구성 (chromosome rearrangement)
- 줄기세포를 이용한 유전자 기능연구
- 형질전환동물의 제작
- 내재적 유전자 표지
- 특이적인 전이유전자의 첨가
전망과 한계[편집]
미래에는 유전체 교정에 있어서 핵산분해효소의 안전성과 특이성을 높이기 위한 노력이 주를 이룰 것이다. 예를 들어, 원하지 않는 부분에 교정이 일어나는 Off-target 현상을 확인할 수 있는 능력이 높아진다면, 우리는 그것을 막을 수 있는 방법을 고안해낼 수 있을 것이다. 뿐만 아니라, ZFNs에 이용되는 zinc-fingers는 특이성이 높지 않기 때문에 세포 독성이 있을 수 있다. 그러나, 절단을 위한 서열을 일부 변형하여 특이성을 높여줌으로서 독성을 줄일 수 있다. 또한, Dana Carroll의 연구에 의하면 조작된 핵산분해효소를 이용하는 과정에서 재조합 및 DNA 수선 기술에 대한 전반적인 이해가 높아졌음을 확인할 수 있었다. 미래에는, 2차 타겟을 구별해낼 수 있는 방식이 개발되어 ZFNs를 발현하는 세포로부터 부서진 말단을 인식해내고, 고해상도 염기서열분석을 이용해 그 주변 DNA 서열을 분석해낼 수 있게 될 것으로 전망한다.
유전체 편집은 인위적인 유전자 조작 뿐만 아니라 자연스러운 과정으로서도 일어난다. 바이러스 또는 바이러스의 일부를 이루는 RNA 매개체는 유전암호를 편집할 수 있는 능력이 있는 것으로 알려져 있다.[25] 하지만, 원하는 변이를 얻을 수 있는 확률은 매우 낮다는 것을 염두에 두어야 한다. 예를 들어, 누군가 세포가 NHEJ에 의한 변이를 만들고자 계획 하였을지라도, 세포는 이중가닥절단을 수선하기 위해 HR을 채택할 수 있는 것이다.
참고 문헌[편집]
- ↑ Esvelt, KM.; Wang, HH. (2013). “Genome-scale engineering for systems and synthetic biology.”. 《Mol Syst Biol》 9 (1): 641. doi:10.1038/msb.2012.66. PMC 3564264. PMID 23340847.
- ↑ Tan, WS.; Carlson, DF.; Walton, MW.; Fahrenkrug, SC.; Hackett, PB. (2012). “Precision editing of large animal genomes.”. 《Adv Genet》 80: 37–97. doi:10.1016/B978-0-12-404742-6.00002-8. PMC 3683964. PMID 23084873.
- ↑ Puchta, H.; Fauser, F. (2013). “Gene targeting in plants: 25 years later.”. 《Int. J. Dev. Biol》 57: 629–637. doi:10.1387/ijdb.130194hp.
- ↑ Capecchi, M., Altering the genome by homologous recombination" Science 244 (4910), 1288-1292 (1989).
- ↑ 이동:가 나 다 Silvana B. De Lorenzo; Anand G. Patel; Rachel M. Hurley; Scott H. Kaufmann. “The elephant and the blind men: making sense of PARP inhibitors in homologous recombination deficient tumor cells”. 《Frontiers in oncology》.
- ↑ Gong, C. et al., Mechanism of nonhomologous end-joining in mycobacteria: a low-fidelity repair system driven by Ku, ligase D and ligase C. Nat Struct Mol Biol 12 (4), 304-312 (2005).
- ↑ Feyruz Virgilia, R., DNA double strand breaks (DSB) and non-homologous end joining (NHEJ) pathways in human leukemia. Cancer Letters 193 (1), 1-9 (2003).
- ↑ Maria, J., Genetic manipulation of genomes with rare-cutting endonucleases" Trends in Genetics 12 (6), 224-228 (1996).
- ↑ de Souza, N., Primer: genome editing with engineered nucleases. Nat Meth 9 (1), 27-27 (2011).
- ↑ 이동:가 나 다 Smith, J. et al., A combinatorial approach to create artificial homing endonucleases cleaving chosen sequences" Nucleic Acids Research 34 (22), e149 (2006).
- ↑ Chevalier, B.S. et al., Design, Activity, and Structure of a Highly Specific Artificial Endonuclease" Molecular Cell 10 (4), 895-905 (2002).
- ↑ “Baker M (January 2012). "Gene-editing nucleases". Nature Methods. 9 (1): 23–6. PMID 22312637.”.
- ↑ “Kim YG, Cha J, Chandrasegaran S (February 1996). "Hybrid restriction enzymes: zinc finger fusions to Fok I cleavage domain". Proceedings of the National Academy of Sciences of the United States of America. 93 (3): 1156–60. doi:10.1073/pnas.93.3.1156. PMC 40048 Freely accessible. PMID 8577732.”.
- ↑ “Urnov FD, Rebar EJ, Holmes MC, Zhang HS, Gregory PD (September 2010). "Genome editing with engineered zinc finger nucleases". Nature Reviews. Genetics. 11 (9): 636–46. doi:10.1038/nrg2842. PMID 20717154.”.
- ↑ “Urnov FD, Rebar EJ, Holmes MC, Zhang HS, Gregory PD (September 2010). "Genome editing with engineered zinc finger nucleases". Nature Reviews. Genetics. 11 (9): 636–46. doi:10.1038/nrg2842. PMID 20717154.”.
- ↑ “de Souza N (January 2012). "Primer: genome editing with engineered nucleases". Nature Methods. 9 (1): 27. doi:10.1038/nmeth.1848. PMID 22312638.”.
- ↑ Stella, Stefano; Montoya, Guillermo (2016년 7월 1일). “The genome editing revolution: A CRISPR-Cas TALE off-target story”. 《BioEssays》 (영어) 38: S4–S13. doi:10.1002/bies.201670903. ISSN 1521-1878.
- ↑ Bogdanove, Adam J.; Voytas, Daniel F. (2011년 9월 30일). “TAL Effectors: Customizable Proteins for DNA Targeting”. 《Science》 (영어) 333 (6051): 1843–1846. doi:10.1126/science.1204094. ISSN 0036-8075. PMID 21960622.
- ↑ Holkers, Maarten; Maggio, Ignazio; Liu, Jin; Janssen, Josephine M.; Miselli, Francesca; Mussolino, Claudio; Recchia, Alessandra; Cathomen, Toni; Gonçalves, Manuel A. F. V. (2013년 3월 1일). “Differential integrity of TALE nuclease genes following adenoviral and lentiviral vector gene transfer into human cells”. 《Nucleic Acids Research》 (영어) 41 (5): e63–e63. doi:10.1093/nar/gks1446. ISSN 0305-1048.
- ↑ Juillerat, Alexandre; Bertonati, Claudia; Dubois, Gwendoline; Guyot, Valérie; Thomas, Séverine; Valton, Julien; Beurdeley, Marine; Silva, George H.; Daboussi, Fayza (2014년 1월 23일). “BurrH: a new modular DNA binding protein for genome engineering”. 《Scientific Reports》 (영어) 4 (1). doi:10.1038/srep03831. ISSN 2045-2322.
- ↑ Mojica, Francisco J. M.; Díez-Villaseñor, Chc)sar; García-Martínez, Jesús; Soria, Elena (2005년 2월 1일). “Intervening Sequences of Regularly Spaced Prokaryotic Repeats Derive from Foreign Genetic Elements”. 《Journal of Molecular Evolution》 (영어) 60 (2): 174–182. doi:10.1007/s00239-004-0046-3. ISSN 0022-2844.
- ↑ Grissa, Ibtissem; Vergnaud, Gilles; Pourcel, Christine. “The CRISPRdb database and tools to display CRISPRs and to generate dictionaries of spacers and repeats”. 《BMC Bioinformatics》 8 (1). doi:10.1186/1471-2105-8-172. 2018년 4월 23일에 원본 문서에서 보존된 문서. 2018년 4월 23일에 확인함.
- ↑ Jinek, Martin; Chylinski, Krzysztof; Fonfara, Ines; Hauer, Michael; Doudna, Jennifer A.; Charpentier, Emmanuelle (2012년 8월 17일). “A Programmable Dual-RNA–Guided DNA Endonuclease in Adaptive Bacterial Immunity”. 《Science》 (영어) 337 (6096): 816–821. doi:10.1126/science.1225829. ISSN 0036-8075. PMID 22745249.
- ↑ 이동:가 나 McMahon, M.A., Rahdar, M., & Porteus, M., Gene editing: not just for translation anymore. Nat Meth 9 (1), 28-31 (2012).
- ↑ Witzany, G (2011). “The agents of natural genome editing”. 《J Mol Cell Biol》 3 (3): 181–189. doi:10.1093/jmcb/mjr005. PMID 21459884.
'생명공학' 카테고리의 다른 글
| 글로벌 생명과학- Discover Promega (0) | 2023.03.25 |
|---|---|
| 고통 저감 유전자 드라이브 (0) | 2023.02.28 |
| DNA/RNA에서 D/E 반복 (0) | 2023.02.14 |
| NCBI GEO 유전체학 데이터 (0) | 2023.02.14 |
| NCBI 생명 공학 정보 센터 (0) | 2023.02.14 |




